이 기사의 목차 :
1. 아미노산의 발달
2. 구조적 특성
3. 화학 성분
4. 분류
5. 합성
6. 물리 화학적 특성
7. 독성
8. 항균 활성
9. 유변학 적 특성
10. 미용 산업의 응용
11. 일상적인 화장품의 응용
아미노산 계면 활성제 (AAS)소수성기를 하나 이상의 아미노산과 조합하여 형성된 계면 활성제의 종류이다. 이 경우, 아미노산은 합성 또는 단백질 가수 분해물 또는 유사한 재생 가능 공급원으로부터 유래 될 수있다. 이 논문은 AA에 가용 한 합성 경로의 대부분의 세부 사항과 용해도, 분산 안정성, 독성 및 생분해 성을 포함한 최종 생성물의 물리 화학적 특성에 대한 다른 경로의 효과를 다룹니다. 수요가 증가하는 계면 활성제로서, 가변 구조로 인한 AA의 다양성은 많은 상업적 기회를 제공합니다.
계면 활성제가 세제, 유화제, 부식 억제제, 3 차 회수 및 제약에 널리 사용된다는 점을 감안할 때, 연구원들은 계면 활성제에주의를 기울이지 않았다.
계면 활성제는 전 세계적으로 매일 대량으로 소비되는 가장 대표적인 화학 제품이며 수생 환경에 부정적인 영향을 미쳤습니다.연구에 따르면 전통적인 계면 활성제의 광범위한 사용은 환경에 부정적인 영향을 줄 수 있습니다.
오늘날, 비 독성, 생분해 성 및 생체 적합성은 계면 활성제의 유용성과 성능만큼이나 소비자에게는 거의 중요합니다.
생물 계면 활성제는 박테리아, 곰팡이 및 효모와 같은 미생물에 의해 자연적으로 합성되는 환경 친화적으로 지속 가능한 계면 활성제입니다.따라서, 생물 계면 활성제는 또한 분자 설계에 의해 인지질, 알킬 글리코 사이드 및 아실 아미노산과 같은 천연 양친 매성 구조를 모방하기 위해 제조 될 수있다.
아미노산 계면 활성제 (AAS)일반적으로 동물 또는 농업 유래 원료에서 생산되는 전형적인 계면 활성제 중 하나입니다. 지난 20 년 동안 AAS는 재생 가능한 자원으로부터 합성 될 수있을뿐만 아니라 AAS가 쉽게 분해 될 수 있고 무해한 부산물을 가지고 있기 때문에 과학자들로부터 새로운 계면 활성제로서 많은 관심을 끌었습니다.
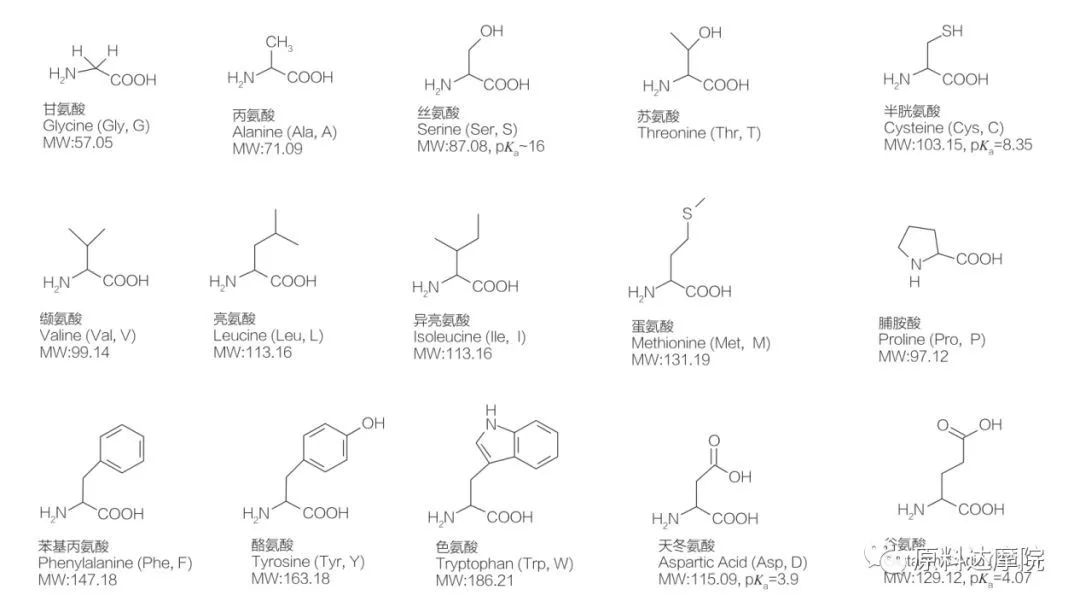
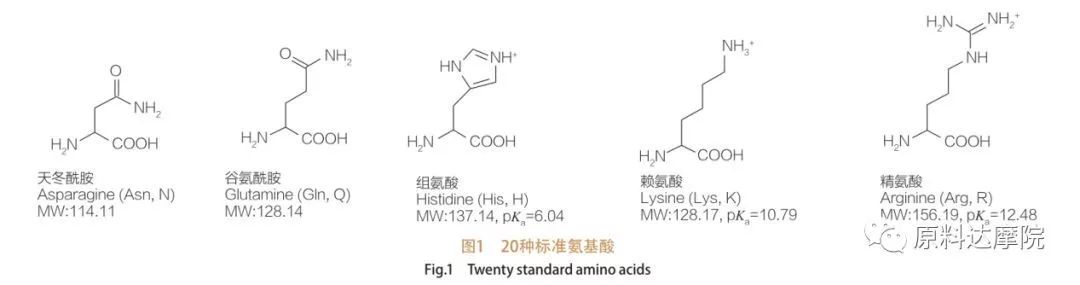
AA는 아미노산을 함유하는 아미노산 (HO 2 C-CHR-NH 2) 또는 아미노산 잔기 (HO 2 C-CHR-NH-)로 구성된 아미노산으로 구성된 계면 활성제로 정의 될 수있다. 아미노산의 2 가지 기능 영역은 다양한 계면 활성제의 유도를 허용한다. 총 20 개의 표준 단백질 생성 아미노산이 자연에 존재하는 것으로 알려져 있으며 성장 및 생명 활동의 모든 생리 학적 반응을 담당합니다. 그것들은 잔기 R에 따라 서로 다릅니다 (그림 1, PK A는 용액의 산 해리 상수의 음의 로그). 일부는 비극성 및 소수성이며 일부는 극성이고 친수성이며 일부는 기본적이며 일부는 산성입니다.
아미노산은 재생 가능한 화합물이기 때문에, 아미노산으로부터 합성 된 계면 활성제는 또한 지속 가능하고 환경 친화적이 될 가능성이 높다. 단순하고 자연적인 구조, 낮은 독성 및 빠른 생분해 성은 종종 종종 계면 활성제보다 우수합니다. 재생 가능한 원료 (예 : 아미노산 및 식물성 오일)를 사용하여 AA는 다른 생명 공학 경로 및 화학 경로에 의해 생산 될 수 있습니다.
20 세기 초, 아미노산은 계면 활성제의 합성을위한 기질로서 처음으로 발견 된 것으로 밝혀졌다.AA는 주로 제약 및 화장품 제형에서 방부제로 사용되었습니다.또한, AAS는 다양한 질병을 유발하는 박테리아, 종양 및 바이러스에 대해 생물학적으로 활성 인 것으로 밝혀졌다. 1988 년에 저렴한 AAS의 가용성은 표면 활동에 대한 연구 관심을 생성했습니다. 오늘날 생명 공학의 발달로 일부 아미노산은 효모에 의해 대규모로 상업적으로 합성 될 수 있으며, 이는 AAS 생산이보다 환경 친화적임을 간접적으로 증명합니다.
01 아미노산의 발달
자연적으로 발생하는 아미노산이 처음 발견 된 19 세기 초반, 그들의 구조는 양서류 제조를위한 원료로 사용 가능한 매우 가치가있는 것으로 예상되었습니다. AAS의 합성에 대한 첫 번째 연구는 1909 년 Bondi에 의해보고되었다.
이 연구에서, N- 아실 글리신 및 N- 아실라닌은 계면 활성제에 대한 친수성 그룹으로 도입되었다. 후속 연구는 글리신과 알라닌을 사용한 리포 아미노산 (AAS)의 합성과 Hentrich et al. 일련의 결과를 발표했습니다.첫 번째 특허 출원을 포함하여, 가정용 세정 제품 (예 : 샴푸, 세제 및 치약)에서 계면 활성제로서 아실 사르코 네이트 및 아실 아스파 테이트 염의 사용.그 후, 많은 연구자들은 아실 아미노산의 합성 및 물리 화학적 특성을 조사했다. 현재까지, AAS의 합성, 특성, 산업 응용 및 생분해성에 관한 많은 문헌이 발표되었습니다.
02 구조적 특성
AA의 비극성 소수성 지방산 사슬은 구조, 사슬 길이 및 수가 다를 수 있습니다.AAS의 구조적 다양성과 높은 표면 활성은 그들의 광범위한 구성 다양성과 물리 화학적 및 생물학적 특성을 설명한다. AA의 헤드 그룹은 아미노산 또는 펩티드로 구성된다. 헤드 그룹의 차이는 이들 계면 활성제의 흡착, 응집 및 생물학적 활성을 결정한다. 그런 다음 헤드 그룹의 기능적 그룹은 양이온 성, 음이온 성, 비 이온 성 및 수륙 양용을 포함한 AA의 유형을 결정합니다. 친수성 아미노산 및 소수성 장쇄 부분의 조합은 양서류 구조를 형성하여 분자를 고도로 활성화시킨다. 또한, 분자에서 비대칭 탄소 원자의 존재는 키랄 분자를 형성하는 데 도움이된다.
03 화학 성분
모든 펩티드 및 폴리펩티드는 이들 거의 20 개의 α- 단백질 α- 아미노산의 중합 생성물이다. 20 개의 α- 아미노산은 모두 동일한 사면체 α- 탄소 원자에 부착 된 카르 복실 산 기능성 그룹 (-COOH) 및 아미노 기능 그룹 (-NH 2)을 함유한다. 아미노산은 α- 탄소에 부착 된 상이한 R 그룹에 의해 서로 다릅니다 (R 그룹이 수소 인 리신 제외). R 그룹은 구조, 크기 및 전하 (산도, 알칼리도)가 다를 수 있습니다. 이러한 차이는 또한 물에서 아미노산의 용해도를 결정합니다.
아미노산은 키랄이며 (글리신 제외), 알파 탄소에 연결된 4 개의 다른 치환기가 있기 때문에 본질적으로 광학적으로 활성화된다. 아미노산은 두 가지 가능한 형태를 갖는다; 그들은 L- 스테레오 이성질체의 수가 상당히 높다는 사실에도 불구하고 서로의 무너지지 않는 거울 이미지입니다. 일부 아미노산 (페닐알라닌, 티로신 및 트립토판)에 존재하는 R- 그룹은 아릴이며, 280 nm에서 최대 UV 흡수를 초래한다. 아미노산의 산성 α-COOH 및 기본 α-NH 2는 이온화가 가능하며, 이들이 무엇이든, 두 입체 이성질체는 아래에 도시 된 이온화 평형을 구성한다.
r-cooh ↔r-coo-h. h+
r-n3+↔r-nh2h. h+
상기의 이온화 평형에서 나타낸 바와 같이, 아미노산은 적어도 2 개의 약한 산성 그룹을 함유하고; 그러나, 카르 복실 그룹은 양성자 화 아미노기에 비해 훨씬 더 산성이다. pH 7.4, 카르 복실 그룹은 아미노기가 양성자 화되는 반면, 카르 복실 그룹은 탈 양성자 화된다. 비 이온화 불가능한 R기를 갖는 아미노산은이 pH에서 전기적으로 중립적이며 형성 Zwitterion이다.
04 분류
AA는 4 가지 기준에 따라 분류 될 수 있으며, 이는 아래에 설명되어 있습니다.
원산지에 따라 4.1
| 원산지에 따르면 AAS는 다음과 같이 두 가지 범주로 나눌 수 있습니다. ① 자연 카테고리 아미노산을 함유하는 일부 자연적으로 발생하는 화합물은 또한 표면/계면 장력을 감소시키는 능력을 가지고 있으며, 일부는 혈당 지질의 효능을 초과한다. 이 AA는 리포 펩티드라고도합니다. 리포 펩티드는 보통 바실러스 종에 의해 생성되는 저 분자량 화합물이다.
이러한 AA는 3 개의 서브 클래스로 더 나뉩니다.Surfactin, Iturin 및 Fengycin.
|
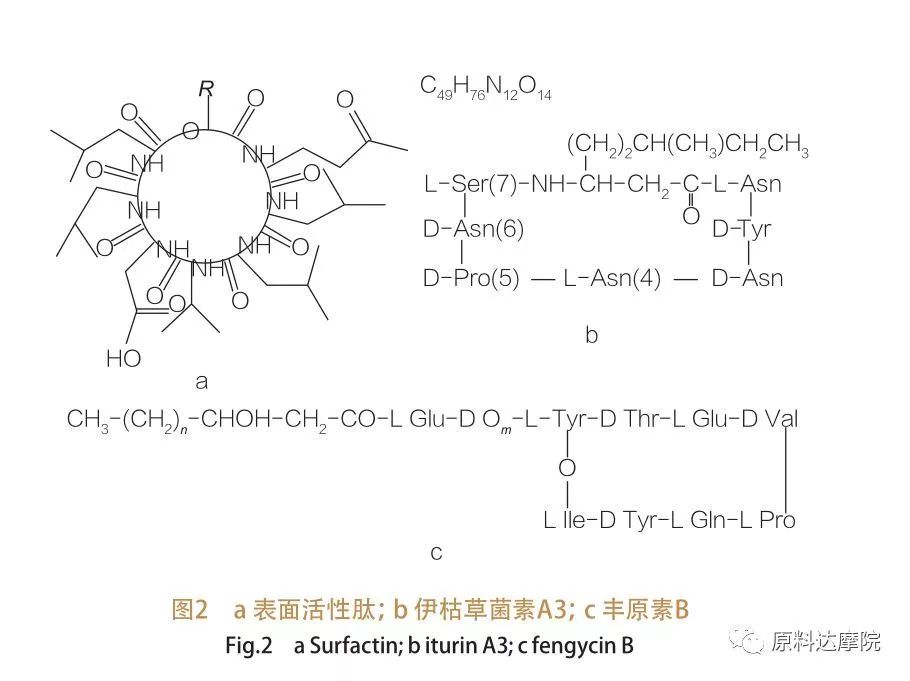
| 표면 활성 펩티드의 패밀리는 다양한 물질의 헵타 펩티드 변이체를 포함합니다.C12-C16 불포화 β- 하이드 록시 지방산 사슬이 펩티드에 연결된도 2a에 도시 된 바와 같이. 표면-활성 펩티드는 β- 하이드 록시 지방산의 C- 말단 및 펩티드 사이의 촉매에 의해 고리가 닫히는 마크로 사이 클릭 락톤이다. Iturin의 서브 클래스에는 6 가지 주요 변이체, 즉 Iturin A 및 C, Mycosubtilin 및 Bacillomycin D, F 및 L이 있습니다.모든 경우에, 헵타 펩티드는 β- 아미노 지방산의 C14-C17 사슬에 연결되어있다 (사슬은 다양 할 수 있음). 에쿠리 마이신의 경우, β- 위치의 아미노기는 C- 말단과 아미드 결합을 형성하여 마크로 사이 클릭 락탐 구조를 형성 할 수있다.
서브 클래스 펜기 세신은 펜지 세신 A 및 B를 함유하며, 이는 Tyr9가 D- 구성 될 때 플리 파스타틴이라고도합니다.데카 펩티드는 C14 -C18 포화 또는 불포화 β- 하이드 록시 지방산 사슬에 연결된다. 구조적으로, Plipastatin은 또한 펩티드 서열의 위치 3에서 Tyr 측쇄를 함유하고 C- 말단 잔기와 에스테르 결합을 형성하여 내부 고리 구조를 형성하는 마크로 사이 클릭 락톤이다 (많은 pseudomonas lipopeptides의 경우).
② 합성 카테고리 AA는 또한 산성, 염기성 및 중성 아미노산을 사용하여 합성 될 수 있습니다. AAS의 합성에 사용되는 일반적인 아미노산은 글루탐산, 세린, 프롤린, 아스파르트 산, 글리신, 아르기닌, 알라닌, 류신 및 단백질 가수 분해물이다. 계면 활성제 의이 서브 클래스는 화학적, 효소 및 화학 엔 자학 적 방법에 의해 제조 될 수있다; 그러나 AAS의 생산의 경우 화학적 합성이 경제적으로 실현 가능합니다. 일반적인 예는 N-Lauroyl-L- 글루탐산 및 N- 팔미 토일 -L- 글루탐산을 포함한다.
|
4.2 지방족 사슬 치환기에 기초합니다
지방족 사슬 치환기에 기초하여, 아미노산 기반 계면 활성제는 2 가지 유형으로 나눌 수있다.
치환의 위치에 따라
| aS- 치환 된 AAS N- 치환 화합물에서, 아미노기는 친 유성 그룹 또는 카르 복실 그룹으로 대체되어 염기성이 상실된다. N- 치환 된 AA의 가장 간단한 예는 본질적으로 음이온 성 계면 활성제 인 N- 아실 아미노산이다. N- 치환 된 AA는 소수성 및 친수성 부분 사이에 부착 된 아미드 결합을 갖는다. 아미드 결합은 수소 결합을 형성하는 능력을 가지고 있으며, 이는 산성 환경 에서이 계면 활성제의 분해를 촉진시켜 생분해 성이됩니다.
aS- 치환 된 AAS C- 치환 된 화합물에서, 치환은 (아미드 또는 에스테르 결합을 통해) 카르복실기에서 발생한다. 전형적인 C- 치환 화합물 (예 : 에스테르 또는 아미드)은 본질적으로 양이온 성 계면 활성제이다.
③n- 및 c- 치환 된 AAS 이러한 유형의 계면 활성제에서, 아미노 및 카르 복실 그룹은 친수성 부분이다. 이 유형은 본질적으로 수륙 양용 계면 활성제입니다. |
4.3 소수성 꼬리의 수에 따라
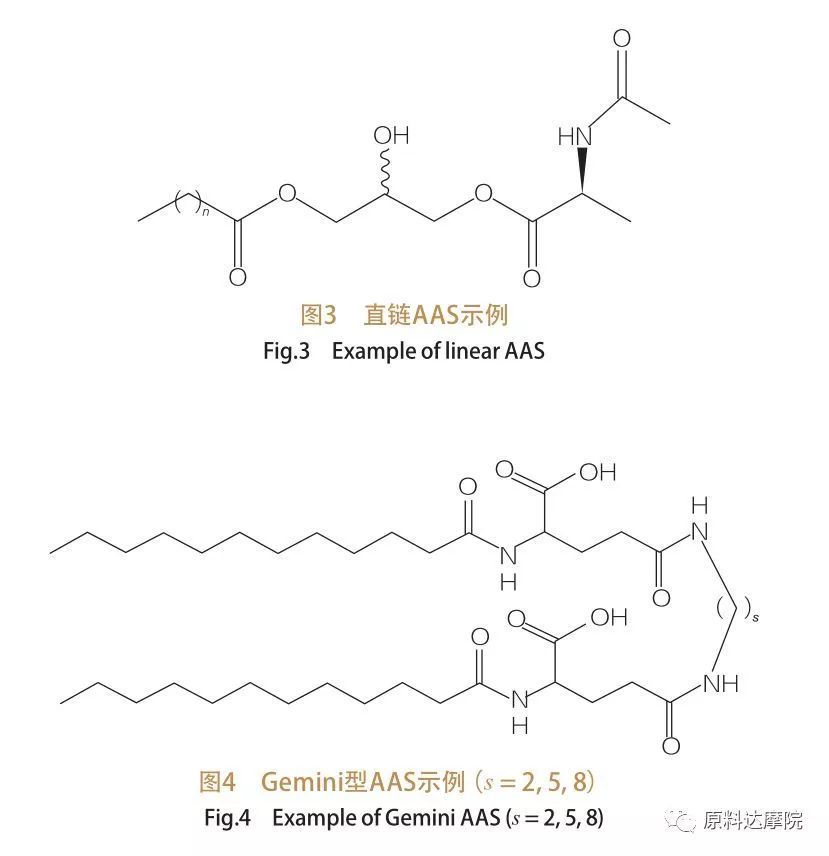
헤드 그룹 및 소수성 꼬리의 수를 기준으로 AA는 4 개의 그룹으로 나눌 수 있습니다. 직선형 AAS, 쌍둥이 자리 (이량 체) 타입 AAS, 글리세로 지질 유형 AA 및 바이스 팔 릭 양서류 (BOLA) 타입 AA. 직선형 계면 활성제는 하나의 소수성 꼬리 만있는 아미노산으로 구성된 계면 활성제이다 (도 3). Gemini 유형 AA는 분자 당 2 개의 아미노산 극성 헤드 그룹과 2 개의 소수성 꼬리를 가지고 있습니다 (그림 4). 이러한 유형의 구조에서, 2 개의 직선형 AA는 스페이서로 연결되므로 이량 체라고도합니다. 반면에, 글리세로 지질 유형 AAS에서, 2 개의 소수성 꼬리는 동일한 아미노산 헤드 그룹에 부착된다. 이들 계면 활성제는 모노 글리세리드, 디 글리세리드 및 인지질의 유사체로 간주 될 수있는 반면, 볼라 형 AAS에서는 2 개의 아미노산 헤드 그룹이 소수성 꼬리에 의해 연결된다.
4.4 헤드 그룹의 유형에 따라
율의 AAS
이 유형의 계면 활성제의 헤드 그룹은 양전하를 갖는다. 가장 초기의 양이온 성 AA는 에틸 코코 일 아르 네이트이며, 이는 피 롤리 돈 카르 복실 레이트이다. 이 계면 활성제의 독특하고 다양한 특성은 소독제, 항 미생물 제, 항성제, 모발 컨디셔너뿐만 아니라 눈과 피부에 부드럽고 쉽게 생분해성에 유용하게 만듭니다. Singare와 Mhatre는 아르기닌 기반 양이온 AAS를 합성하고 그들의 물리 화학적 특성을 평가했습니다. 이 연구에서 그들은 Schotten-Baumann 반응 조건을 사용하여 얻은 제품의 높은 수율을 주장했다. 알킬 사슬 길이 및 소수성이 증가함에 따라, 계면 활성제의 표면 활성이 증가하는 것으로 밝혀졌으며, 임계 미셀 농도 (CMC)가 감소하는 것으로 밝혀졌다. 다른 하나는 4 차 아실 단백질이며, 이는 일반적으로 모발 관리 제품의 컨디셔너로 사용됩니다.
anionic AAS
음이온 성 계면 활성제에서, 계면 활성제의 극성 헤드 그룹은 음전하를 갖는다. 성게 및 바다 별에서 흔히 발견되는 아미노산 인 사르코신 (CH 3 -NH -COOH, N- 메틸 글리신)은 포유 동물 세포에서 발견되는 기본 아미노산 인 글리신 (NH 2 -CH 2 -COOH)과 화학적으로 관련이있다. -cooh,)는 포유 동물 세포에서 발견되는 기본 아미노산 인 글리신과 화학적으로 관련이 있습니다. 로릭 산, 테트라 데카 노산, 올레산 및 이들의 할라이드 및 에스테르는 일반적으로 사르코 네이트 계면 활성제를 합성하는 데 사용됩니다. Sarcosinates는 본질적으로 온화하므로 구강 세척제, 샴푸, 스프레이 면도 거품, 선 스크린, 피부 클렌저 및 기타 화장품에 일반적으로 사용됩니다.
다른 상업적으로 이용 가능한 음이온 성 AA에는 각각 나트륨 N-Cocoyl-L-Glutamate 및 칼륨 N- 코실 글리시 네이트의 상표 이름 인 Amisoft CS-22 및 AmiliteGCK-12가 포함됩니다. 아밀 라이트는 일반적으로 발포제, 세제, 가용화제, 유화제 및 분산제로 사용되며 샴푸, 욕조 비누, 바디 워시, 치약, 얼굴 클렌저, 클렌징 렌즈 클리너 및 가정용 계면 활성제와 같은 화장품에 많은 응용이 있습니다. Amisoft는 주로 얼굴 및 신체 클렌저, 블록 합성 세제, 바디 케어 제품, 샴푸 및 기타 스킨 케어 제품에서 온화한 피부 및 헤어 클렌저로 사용됩니다.
zwitterionic 또는 Amphoteric AAS
양서류 계면 활성제는 산성 및 기본 부위를 모두 함유하므로 pH 값을 변경하여 전하를 변경할 수 있습니다. 알칼리성 매체에서 그들은 음이온 성 계면 활성제처럼 행동하는 반면, 산성 환경에서는 양이온 성 계면 활성제와 양서적 계면 활성제와 같은 중성 매체에서 행동합니다. Lauryl Lysine (LL) 및 알콕시 (2- 하이드 록시 프로필) 아르기닌은 아미노산에 기초한 유일한 양쪽성 계면 활성제이다. LL은 라이신과 로릭 산의 응축 산물입니다. 양서류 구조로 인해 LL은 매우 알칼리성 또는 산성 용매를 제외하고는 거의 모든 유형의 용매에 불용성입니다. 유기 분말로서, LL은 친수성 표면에 대한 우수한 접착력 및 낮은 마찰 계수를 가지 므로이 계면 활성제는 우수한 윤활 능력을 제공합니다. LL은 스킨 크림과 헤어 컨디셔너에 널리 사용되며 윤활제로도 사용됩니다.
nononionic AAS
비 이온 성 계면 활성제는 공식적인 전하가없는 극성 헤드 그룹을 특징으로한다. Al-Sabagh et al. 오일 가용성 α- 아미노산에서. 이 과정에서, L- 페닐알라닌 (LEP) 및 L- 류신을 먼저 헥사 데카 놀로 에스테르 화 한 후 팔미 산으로 인한 후에 2 개의 아미드와 2 개의 에스테르의 α- 아미노산을 제공 하였다. 이어서, 아미드 및 에스테르는 에틸렌 옥사이드와의 축합 반응을 일으켜 상이한 수의 폴리 옥시 에틸렌 단위 (40, 60 및 100)를 갖는 3 개의 페닐알라닌 유도체를 제조 하였다. 이 비 이온 AA는 우수한 세제 및 폼 특성을 가진 것으로 밝혀졌습니다.
05 합성
5.1 기본 합성 경로
AAS에서, 소수성 그룹은 아민 또는 카르 복실 산 부위 또는 아미노산의 측쇄를 통해 부착 될 수있다. 이를 기반으로,도 5에 도시 된 바와 같이 4 개의 기본 합성 경로가 이용 가능하다.
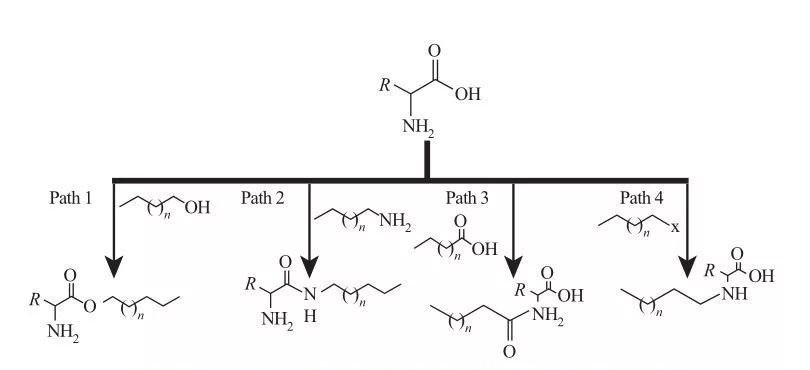
그림 5 아미노산 기반 계면 활성제의 기본 합성 경로
| 경로 1. 양친 매성 에스테르 아민은 에스테르 화 반응에 의해 생성되며,이 경우 계면 활성제 합성은 일반적으로 탈수 제 및 산성 촉매의 존재하에 지방성 알코올 및 아미노산을 환류시킴으로써 달성된다. 일부 반응에서, 황산은 촉매 및 탈수제로서 작용한다.
경로 2. 활성화 된 아미노산은 알킬 아민과 반응하여 아미드 결합을 형성하여 양친 매성 아미도 아민의 합성을 초래한다.
경로 3. 아미도 산은 아미노산의 아민기를 아미 도산과 반응시킴으로써 합성된다.
경로 4. 장쇄 알킬 아미노산은 아민 기의 헤일로 알칸과의 반응에 의해 합성되었다. |
5.2 합성 및 생산의 발전
5.2.1 단일 체인 아미노산/펩티드 계면 활성제의 합성
N- 아실 또는 O- 아실 아미노산 또는 펩티드는 지방산을 갖는 아민 또는 하이드 록실기의 효소-촉매 아실화에 의해 합성 될 수있다. 아미노산 아미드 또는 메틸 에스테르 유도체의 용매가없는 리파제-촉매 합성에 대한 최초의 보고서는 칸디다 남극을 사용했으며, 수율은 표적 아미노산에 따라 25% 내지 90% 범위이다. 메틸 에틸 케톤은 또한 일부 반응에서 용매로서 사용되어왔다. Vonderhagen et al. 또한 물 및 유기 용매 (예 : 디메틸 포름 아미드/물) 및 메틸 부틸 케톤의 혼합물을 사용하여 아미노산, 단백질 가수 분해물 및/또는 이들의 유도체의 리파제 및 프로테아제-촉매 N- 아실화 반응을 기술했다.
초기에, AA의 효소 촉매 합성의 주요 문제는 낮은 수율이었다. Valivety et al. N- 테트라 데카 노일 아미노산 유도체의 수율은 상이한 리파제를 사용하고 70 ℃에서 며칠 동안 인큐베이션 한 후에도 2% -10%에 불과했다. Montet et al. 또한 지방산과 식물성 오일을 사용한 N- 아실 라이신의 합성에서 아미노산의 낮은 수율에 관한 문제가 발생했다. 이들에 따르면, 제품의 최대 수율은 용매가없는 조건과 유기 용매를 사용 하에서 19%였다. Valivety et al.에 의해 동일한 문제가 발생했습니다. N-CBZ-L- 리신 또는 N-CBZ- 리신 메틸 에스테르 유도체의 합성에서.
이 연구에서 그들은 N- 보호 된 세린을 기질로 사용하고 Novozyme 435를 용융 된 용매가없는 환경에서 촉매로 사용할 때 3-O- 테트라 데카 노일 -L- 세린의 수율이 80%라고 주장했다. Nagao 및 Kito는 리파제를 사용할 때 L- 세린, L- 호모 세린, L- 트레오닌 및 L- 티로신 (LET)의 O- 아실화를 연구 하였다 (Lipase는 칸디다 실린 드라시아 및 수성 완충제에서 칸디다 실린 드라 케아 및 rhizopus 디마르에 의해 얻어졌다) 및 Locyin의 아실화의 수확량은 Lo.-Homoserine의 아실화를보고했다고보고했다. L- 트레오닌의 및 왼쪽이 발생했습니다.
많은 연구자들은 비용 효율적인 AAS의 합성을 위해 저렴하고 쉽게 이용 가능한 기질의 사용을 지원했습니다. 수 등 팜유 기반 계면 활성제의 제조는 고정화 된 리포인자임과 가장 잘 작용한다고 주장했다. 그들은 시간이 많이 걸리는 반응 (6 일)에도 불구하고 제품의 수율이 더 좋을 것이라고 언급했다. Gerova et al. 주기적/라 세미 혼합물에서 메티오닌, 프롤린, 류신, 트레오닌, 페닐알라닌 및 페닐 글리신에 기초한 키랄 N- 팔미 토일 AAS의 합성 및 표면 활성을 조사 하였다. PANG 및 ChU는 용액에서 아미노산 기반 단량체 및 디카르 복실 산 기반 단량체의 합성을 기술의 공동 응집 반응에 의해 합성 하였다.
Cantaeuzene과 Guerreiro는 BOC-ALA-OH 및 BOC-ASP-OH의 카르 복실 산 그룹의 에스테르 화를 촉매제로서 용매 및 아고 로스 4B (세 파로스 4B)와 함께 장쇄 지방족 알코올 및 디올로 BOC-ASP-OH의 에스테르 화를보고했다. 이 연구에서, BOC-ALA-OH의 지방 알코올과 최대 16 개의 탄수화물과의 반응은 좋은 수율 (51%)을, BOC-ASP-OH 6 및 12 개의 탄소의 경우 63%의 수율로 더 좋았다 [64]. 99.9%)는 58%내지 76%범위의 수율로, 이는 Papain이 촉매로서 작용 한 CBZ-ARG-OME에 의해 다양한 장쇄 알킬 아민 또는 에스테르 결합과 아미드 결합의 형성에 의해 합성되었다.
5.2.2 쌍둥이 자리 기반 아미노산/펩티드 계면 활성제의 합성
아미노산 기반 쌍둥이 자리 계면 활성제는 스페이서 그룹에 의해 서로 머리-머리와 연결된 2 개의 직선형 AAS 분자로 구성됩니다. 쌍둥이 자리 유형 아미노산 기반 계면 활성제의 화학성 합성에 대한 2 개의 가능한 계획이있다 (도 6 및 7). 도 6에서, 2 개의 아미노산 유도체는 스페이서 그룹으로서 화합물과 반응하고 2 개의 소수성 기가 도입된다. 도 7에서, 2 개의 직선형 구조는 이작 용성 스페이서 그룹에 의해 직접 연결된다.
Gemini 리포 아미노산의 효소-촉매 합성 합성의 초기 발달은 Valivety et al에 의해 개척되었다. Yoshimura et al. 시스틴 및 N- 알킬 브로마이드에 기초한 아미노산 기반 쌍둥이 자리 계면 활성제의 합성, 흡착 및 응집을 조사 하였다. 합성 된 계면 활성제를 상응하는 단량체 계면 활성제와 비교 하였다. Faustino et al. L- 시스트틴, D- 시스트 틴, DL- 시스트 틴, L- 시티 틴, L- 메티오닌 및 L- 설포 알라닌에 기초한 음이온 성 요소 기반 단량체 AAS 및 이들의 전도성, 평형 표면 장력 및 이들의 형광 특성에 의해 Gemini의 합성을 기술했다. 단량체와 쌍둥이 자리를 비교함으로써 쌍둥이 자리의 CMC 값이 더 낮다는 것이 밝혀졌다.
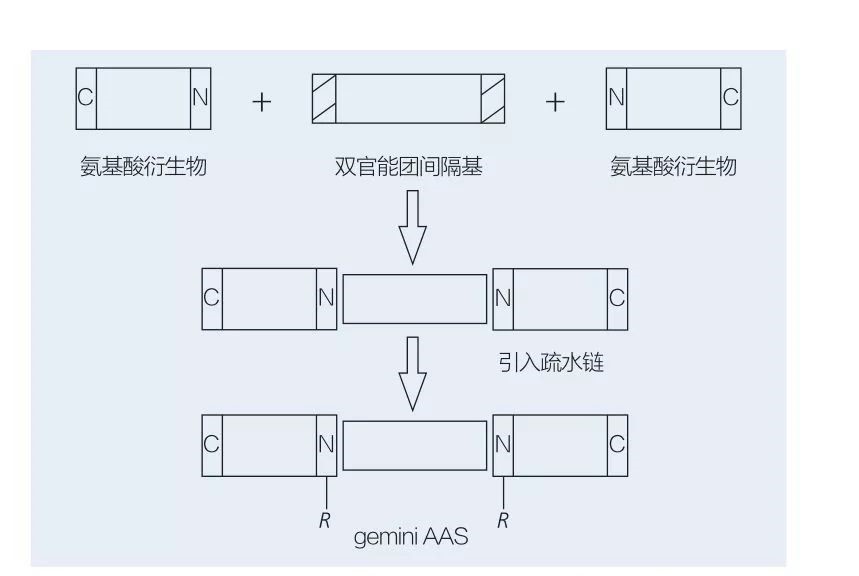
그림 6 AA 유도체 및 스페이서를 사용한 Gemini AA의 합성, 소수성 그룹의 삽입
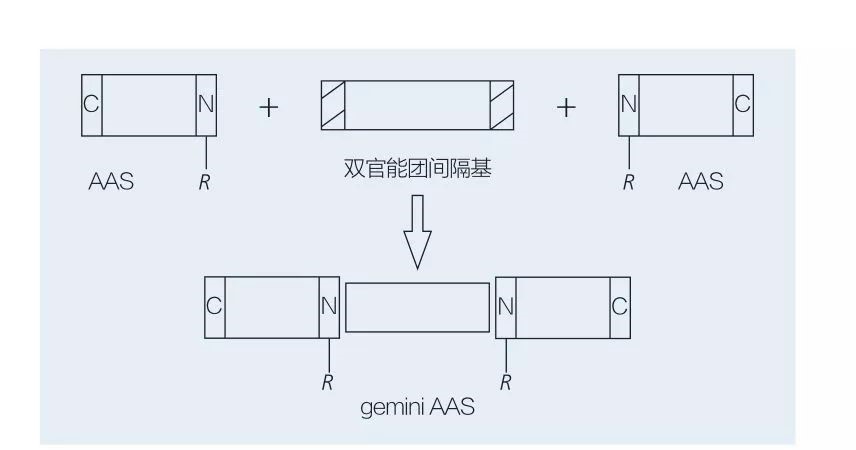
그림 7 이조 장애 스페이서 및 AAS를 사용한 Gemini AAS의 합성
5.2.3 글리세로 질 아미노산/펩티드 계면 활성제의 합성
글리세로 지질 아미노산/펩티드 계면 활성제는 에스테르 결합에 의한 글리세롤 골격에 연결된 하나 또는 2 개의 지방 사슬의 구조로 인해 글리세롤 모노- (또는 디-) 에스테르 및 인지질의 구조적 유사체 인 새로운 종류의 지질 아미노산이다. 이들 계면 활성제의 합성은 높은 온도 및 산성 촉매의 존재하에 아미노산의 글리세롤 에스테르의 제조에서 시작한다 (예 : BF 3). 효소-촉매 합성 합성 (가수 분해 효소, 프로테아제 및 리파제를 사용하여 촉매로서)도 좋은 옵션이다 (도 8).
파파인을 사용한 딜라 릴화 아르기닌 글리세리드 접합체의 효소-촉매 합성이보고되었다. 아세틸 아르기닌으로부터의 디아 실 글리세롤 에스테르 접합체의 합성 및 그들의 물리 화학적 특성의 평가가 또한보고되었다.
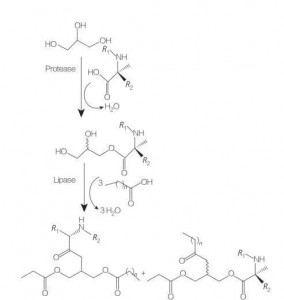
그림 8 모노 및 디아 실 글리세롤 아미노산 접합체의 합성
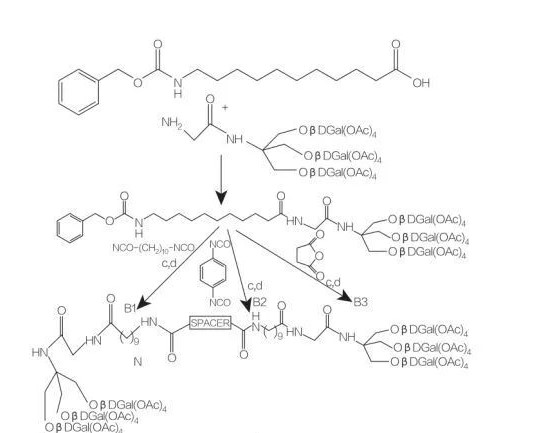
스페이서 : NH- (ch2)10-NH : CompoundB1
스페이서 : NH-C6H4-NH : CompoundB2
스페이서 : ch2-Ch2: compoundb3
그림 9 트리스 (하이드 록시 메틸) 아미노 메탄으로부터 유래 된 대칭 양서류의 합성
5.2.4 볼라 기반 아미노산/펩티드 계면 활성제의 합성
아미노산 기반 볼라 형 옥시 파일은 동일한 소수성 사슬에 연결된 2 개의 아미노산을 함유한다. Franceschi et al. 2 개의 아미노산 (D- 또는 L- 알라닌 또는 L- 시티 딘) 및 상이한 길이의 1 개의 알킬 사슬을 갖는 BOLA- 타입 양서류의 합성을 설명하고 표면 활성을 조사 하였다. 그들은 아미노산 분획 (드물지 않은 β- 아미노산 또는 알코올 사용) 및 C12-C20 스페이서 그룹을 갖는 신규 볼라 형 amphiphile의 합성 및 응집에 대해 논의한다. 사용되지 않은 β- 아미노산은 설탕 아미노아이드, 아지도 디민 (AZT) 유래 아미노산, 노르 보르 넨 아미노산 및 AZT로부터 유래 된 아미노 알코올 일 수있다 (도 9). 트리스 (하이드 록시 메틸) 아미노 메탄 (TRIS)으로부터 유래 된 대칭 볼라 형 옥시 파일의 합성 (도 9).
06 물리 화학적 특성
아미노산 기반 계면 활성제 (AAS)는 본질적으로 다양하고 다재다능하며 우수한 가용성, 우수한 유화 특성, 고효율, 높은 표면 활동 성능 및 경수에 대한 우수한 내성 (칼슘 이온 내성)과 같은 많은 응용 분야에서 적용 가능성이 우수하다는 것이 잘 알려져 있습니다.
아미노산의 계면 활성제 특성 (예 : 표면 장력, CMC, 위상 거동 및 크래프트 온도)에 기초하여, 광범위한 연구 후에 다음 결론에 도달했다.
6.1 중요한 미셀 농도 (CMC)
임계 미셀 농도는 계면 활성제의 중요한 파라미터 중 하나이며 가용화, 세포 용해 및 바이오 필름 등과의 상호 작용과 같은 많은 표면 활성 특성을 제어하여 일반적으로 탄화수소 꼬리의 사슬 길이 (수소 생산성 증가)를 증가 시키면 표면 활성의 CMC 값이 감소합니다. 아미노산에 기초한 계면 활성제는 일반적으로 종래의 계면 활성제와 비교하여 더 낮은 CMC 값을 갖는다.
헤드 그룹 및 소수성 꼬리의 상이한 조합을 통해 (모노 양이온 아미드, 바이 양이온 아미드, 이중 양이온 성 아미드 기반 에스테르), Infante et al. 3 개의 아르기닌 기반 AAS를 합성하고 CMC 및 γCMC (CMC에서 표면 장력)를 연구하여 CMC 및 γCMC 값이 소수성 꼬리 길이가 증가함에 따라 감소 함을 보여 주었다. 다른 연구에서, Singare와 Mhatre는 N-α- 아실라기닌 계면 활성제의 CMC가 소수성 꼬리 탄소 원자의 수를 증가시켜 감소 함을 발견했다 (표 1).
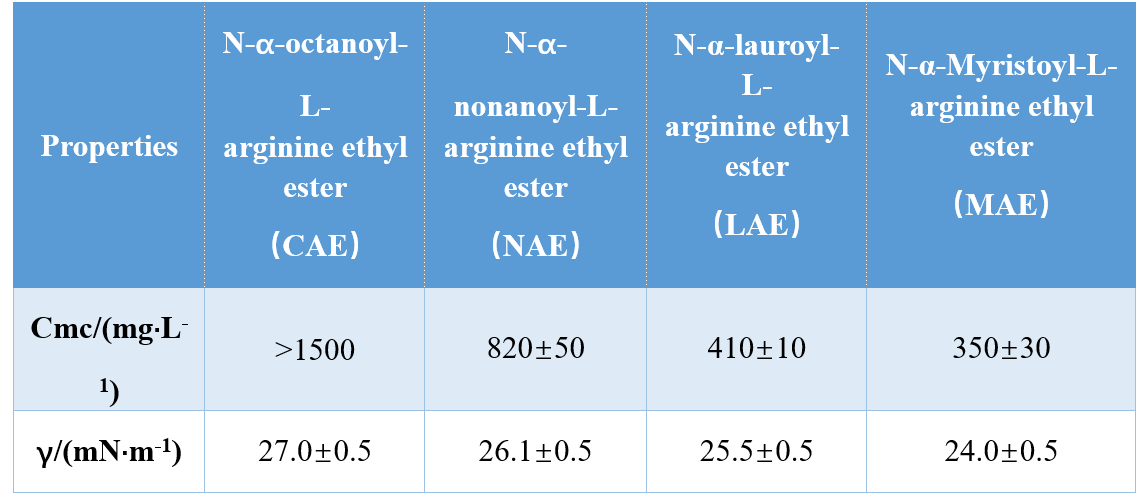
Yoshimura et al. 시스테인 유래 아미노산 기반 쌍둥이 자리 계면 활성제의 CMC를 조사하고, 소수성 사슬의 탄소 사슬 길이가 10에서 12로 증가했을 때 CMC가 감소했음을 보여 주었다.
Faustino et al. 시스틴에 기초한 음이온 성 gemini 계면 활성제의 수용액에서 혼합 미셀의 형성을보고했다. Gemini 계면 활성제는 또한 상응하는 종래의 단량체 계면 활성제 (C 8 Cys)와 비교되었다. 지질-계면 활성제 혼합물의 CMC 값은 순수한 계면 활성제의 값보다 낮은 것으로보고되었다. 수용성, 미셀 형성 인지질 인 인 쌍둥이 자리 계면 활성제 및 1,2- 디 하프 타 노일 -SN- 글리실 -3- 포스 포 콜린은 밀리 몰 수준에서 CMC를 가졌다.
Shrestha와 Aramaki는 혼합 염의 부재하에 혼합 아미노산 기반 음이온 성-비오니니온 성 계면 활성제의 수성 용액에서 점탄성 웜 유사 미셀의 형성을 조사했다. 이 연구에서, N- 도데 실 글루타메이트는 더 높은 크래프트 온도를 갖는 것으로 밝혀졌다; 그러나, 기본 아미노산 L- 리신으로 중화 될 때, 미셀을 생성하고 용액은 25 ℃에서 뉴턴 유체처럼 작동하기 시작했다.
6.2 좋은 물 용해도
AAS의 우수한 물 용해도는 추가적인 공동 결합의 존재 때문입니다. 이는 AAS를 해당 종래의 계면 활성제보다 생분해 성 및 환경 친화적으로 만듭니다. N- 아실 -L- 글루탐산의 수용성은 2 개의 카르 복실기로 인해 더 우수하다. CN (CA) 2의 수용성은 또한 1 분자에 2 개의 이온 성 아르기닌 기가 있기 때문에 양호하며, 이는 세포 계면에서보다 효과적인 흡착 및 확산 및 심지어 낮은 농도에서의 효과적인 박테리아 억제를 초래한다.
6.3 크래프트 온도 및 크래프트 포인트
크래프트 온도는 용해도가 특정 온도보다 급격히 증가하는 계면 활성제의 특정 용해도 거동으로 이해 될 수 있습니다. 이온 성 계면 활성제는 고체 수화물을 생성하는 경향이 있으며, 이는 물에서 침전 될 수 있습니다. 특정 온도 (소위 크래프트 온도)에서, 계면 활성제의 용해도의 극적이고 불연속적인 증가가 관찰된다. 이온 계면 활성제의 크래프트 점은 CMC에서의 크래프트 온도이다.
이 용해도 특성은 일반적으로 이온 성 계면 활성제에 대해 볼 수 있으며 다음과 같이 설명 될 수 있습니다. 계면 활성제 자유 단량체의 용해도는 크래프트 포인트에 도달 할 때까지 크래프트 온도 아래로 제한되어 있으며, 여기서 용해도는 미셀 형성으로 인해 점차 증가합니다. 완전한 용해도를 보장하려면 크래프트 포인트 위의 온도에서 계면 활성제 제형을 준비해야합니다.
AAS의 크래프트 온도는 기존의 합성 계면 활성제의 연구와 비교되어왔다. Shrestha와 Aramaki는 아르기닌 기반 AA의 크래프트 온도를 연구하고 임계 미셀 농도는 2-5 × 10-10 mol-l-1 이상의 프리 미셀 형태로 응집 거동을 나타낸다는 것을 발견했다. 크래프트 온도와 아미노산 잔기 사이의 관계에 대해 논의했다.
실험에서, N- 헥사 데카 노일 AAS의 크래프트 온도는 아미노산 잔기의 크기가 감소함에 따라 증가한 반면 (페닐알라닌은 예외 임), 용해도의 열 (열 흡수)은 아미노산 잔기의 크기가 감소함에 따라 증가하는 것으로 밝혀졌다 (글리신 및 페닐 라닌을 제외하고). 알라닌 및 페닐알라닌 시스템 둘 다에서, DL 상호 작용은 고체 형태의 N-Hexadecanoyl AAS Salt에서 LL 상호 작용보다 강하다고 결론 지었다.
Brito et al. 차등 주사 미세 칼로리 측정법을 사용하여 3 개의 신규 아미노산 기반 계면 활성제의 크래프트 온도를 결정하고, 트리 플루오로 아세테이트 이온을 요오드화물 이온으로 변경하면 크래프트 온도 (약 6 ℃)가 47 ℃에서 53 ℃로 크게 증가 함을 발견했다. 시스-더블 결합의 존재 및 장쇄 공립-유학에 존재하는 불포화는 크래프트 온도의 현저한 감소를 초래했다. N- 도데 실 글루타메이트는 더 높은 크래프트 온도를 갖는 것으로보고되었다. 그러나, 염기성 아미노산 L- 리신으로의 중화는 25 ℃에서 뉴턴 유체처럼 작용하는 용액에서 미셀을 형성시켰다.
6.4 표면 장력
계면 활성제의 표면 장력은 소수성 부분의 사슬 길이와 관련이있다. Zhang et al. Wilhelmy 플레이트 방법 (25 ± 0.2) ° C에 의한 나트륨 코코 일 글리 세미 네이트의 표면 장력을 측정하고 CMC에서 33mn -M -1, CMC에서 0.21 mmol -L -1로 표면 장력 값을 측정 하였다. Yoshimura et al. 2C N Cys 기반 표면 활성제의 2C N Cys 유형 아미노산 기반 표면 장력의 표면 장력을 결정 하였다. CMC에서의 표면 장력은 체인 길이가 증가함에 따라 감소한 반면 (n = 8까지), 추세는 n = 12 이상의 체인 길이로 계면 활성제에 대해 역전 된 것으로 밝혀졌다.
디카 르 복실화 된 아미노산 기반 계면 활성제의 표면 장력에 대한 CAC1 2의 효과가 또한 연구되었다. 이들 연구에서, CAC1 2를 3 개의 디카르 복실화 된 아미노산-타입 계면 활성제 (C12 Malna 2, C12 ASPNA 2 및 C12 Gluna 2)의 수용액에 첨가 하였다. CMC 후의 고원 값을 비교하고 표면 장력이 매우 낮은 CAC1 2 농도에서 감소하는 것으로 밝혀졌다. 이는 가스-물 계면에서 계면 활성제의 배열에 대한 칼슘 이온의 영향 때문이다. 반면에, N- 도데 실 아미노 말로 네이트 및 N- 도데 실 아스 파르 테이트의 염의 표면 긴장은 또한 거의 10 mmol-L -1 CAC1 2 농도까지 거의 일정 하였다. 10 mmol -L -1 이상으로, 계면 활성제의 칼슘 염의 침전의 형성으로 인해 표면 장력이 급격히 증가한다. N- 도데 실 글루타메이트의 단식 염의 경우, CAC1 2의 적당한 첨가는 표면 장력의 현저한 감소를 초래 한 반면, CAC1 2 농도의 지속적인 증가는 더 이상 상당한 변화를 일으키지 않았다.
가스-물 계면에서 Gemini-Type AA의 흡착 동역학을 결정하기 위해, 동적 표면 장력은 최대 기포 압력 방법을 사용하여 결정되었다. 결과는 가장 긴 테스트 시간 동안 2C 12 CYS 동적 표면 장력이 변하지 않았 음을 보여 주었다. 동적 표면 장력의 감소는 농도, 소수성 꼬리의 길이 및 소수성 꼬리의 수에만 의존합니다. 계면 활성제의 농도 증가, 체인 길이 감소 및 사슬의 수는 더 빠른 붕괴를 초래했습니다. 더 높은 농도의 C N Cys (n = 8 내지 12)에 대해 얻어진 결과는 Wilhelmy 방법에 의해 측정 된 γ CMC에 매우 가깝습니다.
다른 연구에서, 나트륨 딜라 릴 시스틴 (SDLC) 및 나트륨 디데 카미노 시스틴의 동적 표면 긴장은 Wilhelmy 플레이트 방법에 의해 결정되었고, 또한, 이들의 수성 용액의 평형 표면 긴장은 낙하 부피 방법에 의해 결정되었다. 이황화 결합의 반응은 다른 방법에 의해서도 추가로 조사되었다. Mercaptoethanol을 0.1 mmol -L -1SDLC 용액에 첨가하면 표면 장력이 34mn -1 내지 53mn -M -1로 급격히 증가 하였다. NaClo가 SDLC의 설 폰산 기에 대한 이황화 결합을 산화시킬 수 있기 때문에, NaClo (5 mmol -L -1)가 0.1 mmol -L -1 SDLC 용액에 첨가 될 때 응집체는 관찰되지 않았다. 투과 전자 현미경 및 동적 광 산란 결과는 용액에 응집체가 형성되지 않았 음을 보여 주었다. SDLC의 표면 장력은 20 분의 기간에 걸쳐 34mn -M -1 내지 60mn -M -1로 증가하는 것으로 밝혀졌다.
6.5 이진 표면 상호 작용
생명 과학에서, 다수의 그룹은 가스-물 계면에서 양이온 성 AAS (디아 실 글리세롤 아르기닌 기반 계면 활성제)와 인지질의 혼합물의 진동 특성을 연구하여 결국이 비 이학적 특성이 정전기 상호 작용의 유병률을 유발한다는 결론을 내렸다.
6.6 집계 특성
동적 광산 산란은 일반적으로 CMC 이상의 농도에서 아미노산 기반 단량체 및 쌍둥이 자리 계면 활성제의 응집 특성을 결정하는데 일반적으로 사용되며, 명백한 유체 역학적 직경 DH (= 2r h)를 생성한다. C N Cys 및 2CN Cys에 의해 형성된 응집체는 비교적 크고 다른 계면 활성제에 비해 광범위한 분포를 갖는다. 2C 12 Cys를 제외한 모든 계면 활성제는 전형적으로 약 10 nm의 응집체를 형성한다. 쌍둥이 자리 계면 활성제의 미셀 크기는 단량체 대응 물보다 상당히 더 큽니다. 탄화수소 사슬 길이의 증가는 또한 미셀 크기의 증가를 초래한다. Ohta et al. 수용액에서 N- 도데 데 실-페닐-알라 닐-알라 닐-알라 닐-알라 닐-알라 닐-알라 닐-알라닌 테트라 메틸 암모늄의 응집 특성을 설명하고, 입체 레 이성질체는 수용액에서 동일한 임계 응집 농도를 갖는 것으로 나타났다. Iwahashi et al. 원형 이색성, NMR 및 증기압 삼투압에 의해 조사 된, N-Dodecanoyl-L-Glutamic Acid, N-Dodecanoyl-L-Valine 및 이들의 메틸 에스테르 (예 : Tetrahydrofuran, Acetonitrile, 1,4- 다이 니네 및 1,2-과 에스테르)에서 메틸 에스테르의 키랄 응집체의 형성. 원형 이색성, NMR 및 증기 압력 삼투압에 의해.
6.7 계면 흡착
아미노산 기반 계면 활성제의 계면 흡착 및 기존의 대응 물과의 비교는 또한 연구 방향 중 하나이다. 예를 들어, LET 및 LEP로부터 수득 된 방향족 아미노산의 도데 실 에스테르의 계면 흡착 특성을 조사 하였다. 결과는 LET와 LEP가 각각 가스-액체 계면과 물/헥산 계면에서 낮은 계면 영역을 나타냈다는 것을 보여 주었다.
Bordes et al. 3 개의 디카르 복실화 된 아미노산 계면 활성제의 가스-물 계면에서 용액 거동 및 흡착을 조사 하였다. 도데 실 글루타메이트, 도데 실 아스 파르 테이트 및 아미노 말로 네이트 (각각 2 개의 카르 복실 그룹 사이의 3, 2 및 1 개의 탄소 원자). 이 보고서에 따르면, 디카 르 복실화 계면 활성제의 CMC는 모노 카르 복실화 된 도데 실 글리신 염의 CMC보다 4-5 배 더 높았다. 이는 디카 르 복실화 계면 활성제와 그 안에 아미드 그룹을 통한 이웃 분자 사이의 수소 결합의 형성에 기인한다.
6.8 위상 동작
매우 높은 농도에서 계면 활성제에 대해 등방성 불연속 입방 단계가 관찰된다. 매우 큰 헤드 그룹을 갖는 계면 활성제 분자는 더 작은 양성 곡률의 응집체를 형성하는 경향이있다. Marques et al. 12LYS12/12SER 및 8LYS8/16SER 시스템의 위상 동작을 연구했으며 (그림 10 참조), 결과는 12LYS12/12SER 시스템이 미셀 및 소포성 용액 영역 사이의 위상 분리 구역을 가지고 있음을 보여주고, 8LYS8/16SER 시스템은 8LYS8/16SER 시스템의 연속성 전이 영역과 소형 미세 상 단계 영역을 보여줍니다. 지역). 12LYS12/12SER 시스템의 소포 영역의 경우, 소포는 항상 미셀과 공존하는 반면, 8LYS8/16SER 시스템의 소포 영역에는 소포 만 있습니다.
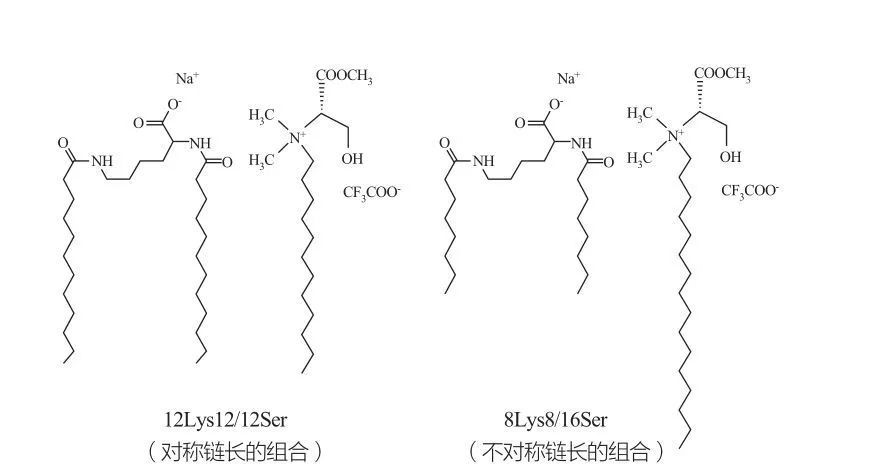
라이신 및 세린 기반 계면 활성제의 촉진제 혼합물 : 대칭 12lys12/12ser 쌍 (왼쪽) 및 비대칭 8LYS8/16SER 쌍 (오른쪽)
6.9 유화 능력
Kouchi et al. N- [3- 도데 실 -2- 하이드 록시 프로필] -L- 아르기닌, L- 글루타메이트 및 기타 AAS의 유화 능력, 계면 장력, 분산 성 및 점도를 조사 하였다. 합성 계면 활성제 (그들의 기존의 비 이온 성 및 양서류 대응 물)와 비교하여, 결과는 AA가 종래의 계면 활성제보다 더 강한 유화 능력을 갖는 것을 보여 주었다.
Baczko et al. 신규 한 음이온 성 아미노산 계면 활성제를 합성하고 키랄 배향 NMR 분광기 용매로서의 적합성을 조사 하였다. 상이한 소수성 꼬리 (Pentyl ~ Tetradecyl)를 갖는 일련의 설포 네이트 기반 양친 매성 L-PHE 또는 L-ALA 유도체를 O-Sulfobenzoic nhydride와 아미노산을 반응시킴으로써 합성되었다. Wu et al. N- 폴트 아실 AAS의 합성 된 나트륨 염 및수체 유화에서의 유화 능력을 조사했으며, 결과는 이들 계면 활성제가 오일 상으로서 N- 헥산보다 오일 상으로서 에틸 아세테이트에서 더 잘 수행되었음을 보여 주었다.
6.10 합성 및 생산의 발전
경수 방수는 계면 활성제가 칼슘 및 마그네슘과 같은 이온의 존재에 저항하는 능력, 즉 칼슘 비누로의 침전을 피하는 능력으로 이해 될 수있다. 강한 방수성이 높은 계면 활성제는 세제 제형 및 개인 관리 제품에 매우 유용합니다. 칼슘 이온의 존재하에 계면 활성제의 용해도 및 표면 활성의 변화를 계산함으로써 경질 방수 저항성을 평가할 수있다.
경질 방수성을 평가하는 또 다른 방법은 물에 분산 될 100g의 나트륨 올리트에서 형성된 칼슘 비누에 필요한 계면 활성제의 백분율 또는 그램을 계산하는 것입니다. 경도가 높은 지역에서는 고농도의 칼슘과 마그네슘 이온 및 미네랄 함량으로 인해 일부 실제 적용을 어렵게 만들 수 있습니다. 종종 나트륨 이온은 합성 음이온 성 계면 활성제의 카운터 이온으로 사용됩니다. 2 차원 이온은 두 계면 활성제 분자에 결합되기 때문에, 계면 활성제는 용액으로부터 더 쉽게 침전되어 세제를 덜 가능하게 만듭니다.
AAS의 경질 방수에 대한 연구에 따르면 산 및 경질 수분 저항은 추가 카르 복실 그룹에 의해 크게 영향을 받았으며, 두 카르 복실 그룹 사이의 스페이서 그룹의 길이가 증가함에 따라 산 및 경질 방수성이 더욱 증가한 것으로 나타났습니다. 산 및 경질 방수의 순서는 C 12 글리시 네이트 <C 12 아스파 테이트 <C 12 글루타메이트였다. 디카 르 복실화 된 아미드 결합 및 디카르 복실화 된 아미노 계면 활성제를 각각 비교하면, 후자의 pH 범위가 더 넓고 표면 활성이 적절한 양의 산을 첨가함에 따라 증가하는 것으로 밝혀졌다. 디카 르 복실화 된 N- 알킬 아미노산은 칼슘 이온의 존재 하에서 킬레이트 효과를 나타냈다. C 12 글루타메이트는 높은 Ca 2+ 농도에서 높은 표면 활성을 보였으며 해수 담수화에 사용될 것으로 예상된다.
6.11 분산 성
분산 성은 용액에서 계면 활성제의 유착 및 퇴적을 방지하기위한 계면 활성제의 능력을 지칭한다.분산 성은 세제, 화장품 및 제약에 사용하기에 적합한 계면 활성제의 중요한 특성입니다.분산 제는 소수성 그룹과 말기 친수성 기 (또는 직선 체인 소수성 기) 사이의 에스테르, 에테르, 아미드 또는 아미노 결합을 함유해야한다.
일반적으로, 알칸 놀라 미도 설페이트와 같은 음이온 성 계면 활성제 및 Amidosulfobetaine과 같은 양서류 계면 활성제는 칼슘 비누에 대한 분산 제로서 특히 효과적이다.
많은 연구 노력으로 N-Lauroyl Lysine은 물과 잘 호환되지 않고 화장품 제형에 사용하기 어려운 AA의 분산 성을 결정했습니다.이 시리즈에서, N- 아실-치환 된 염기성 아미노산은 훌륭한 분산 성을 가지며, 화장품 산업에서 제형을 개선하기 위해 사용된다.
07 독성
기존의 계면 활성제, 특히 양이온 성 계면 활성제는 수생 유기체에 매우 독성이 있습니다. 그들의 급성 독성은 세포-물 계면에서 계면 활성제의 흡착-이온 상호 작용의 현상에 기인한다. 계면 활성제의 CMC를 감소 시키면 일반적으로 계면 활성제의 계면 흡착이 더 강해지며, 이는 일반적으로 급성 독성이 증가합니다. 계면 활성제의 소수성 사슬의 길이의 증가는 또한 계면 활성제 급성 독성의 증가를 초래한다.대부분의 AA는 인간과 환경 (특히 해양 유기체에)에 대해 낮거나 무독성이며 식품 성분, 제약 및 화장품으로 사용하기에 적합합니다.많은 연구자들은 아미노산 계면 활성제가 피부에 부드럽고 변호적이지 않다는 것을 보여주었습니다. 아르기닌 기반 계면 활성제는 기존의 대응 물보다 독성이 적은 것으로 알려져있다.
Brito et al. 아미노산 기반 양친 매성의 물리 화학적 및 독성 학적 특성과 [티로신 (Tyr), 하이드 록시 프롤린 (hyp), 세린 (SER) 및 라이신 (Lys) (Lys)의 자발적 형성 [IC 50)에 대한 자발적 자발적 형성을 연구하고 [IC 50). 이들은 도데 실 트리 메틸 암모늄 브로마이드 (DTAB)/Lys- 유학성 및/또는 Ser-/lys- 유발 성 혼합물의 양이온 성 소포를 합성하고 그들의 생태 독성 및 용혈성 잠재력을 테스트하여 모든 AAS 및 소포 함유 혼합물이 전통적인 계면 활성제 DTAB보다 독성이 적음을 보여 주었다.
Rosa et al. 안정한 아미노산 기반 양이온 성 소포에 대한 DNA의 결합 (연관)을 조사 하였다. 종종 독성이있는 것으로 보이는 종래의 양이온 성 계면 활성제와는 달리, 양이온 성 아미노산 계면 활성제의 상호 작용은 무독성 인 것으로 보인다. 양이온 성 AAS는 아르기닌을 기반으로하며, 이는 특정 음이온 성 계면 활성제와 함께 안정적인 소포를 자발적으로 형성한다. 아미노산 기반 부식 억제제는 또한 무독성으로보고된다. 이들 계면 활성제는 고순도 (최대 99%), 저렴한 비용, 쉽게 생분해 될 수 있으며 수성 매체에 완전히 용해된다. 몇몇 연구에 따르면 황 함유 아미노산 계면 활성제는 부식 억제에서 우수하다는 것이 밝혀졌다.
최근 연구에서 Perinelli et al. 기존의 계면 활성제와 비교하여 rhamnolipids의 만족스러운 독성 학적 프로파일을보고했다. Rhamnolipids는 투과성 향상제로서 작용하는 것으로 알려져있다. 그들은 또한 거대 분자 약물의 상피 투과성에 대한 Rhamnolipids의 효과를보고했다.
08 항균 활성
계면 활성제의 항균 활성은 최소 억제 농도에 의해 평가 될 수있다. 아르기닌 기반 계면 활성제의 항균 활성은 상세하게 연구되었다. 그람 음성 박테리아는 그람 양성 박테리아보다 아르기닌 기반 계면 활성제에 더 내성이있는 것으로 밝혀졌다. 계면 활성제의 항균 활성은 일반적으로 아실 사슬 내에서 하이드 록실, 시클로 프로판 또는 불포화 결합의 존재에 의해 증가된다. Castillo et al. 아실 사슬의 길이와 양전하가 분자의 HLB 값 (친수성-친 유성 균형)을 결정하고, 이들은 막을 방해하는 능력에 영향을 미친다는 것을 보여 주었다. Nα- 아실라기닌 메틸 에스테르는 넓은 스펙트럼 항균 활성을 갖는 양이온 성 계면 활성제의 또 다른 중요한 종류이며, 쉽게 생분해 될 수 있으며 독성이 낮거나 없다. Nα- 아실라기닌 메틸 에스테르 기반 계면 활성제와 1,2- 디 팔미 토일 -SN- 프로필 트리 옥실 -3- 포스 포 콜린 및 1,2- 디트라 드라 데카 노일 -SN- 프로필 트리 옥실 -3- 프로필 트리 옥실 -3- 인산형 콜린, 모델 막, 그리고이 분류에 살고있는 유기체와의 상호 작용에 대한 연구는 1,2- 디 팔미 토일 -SN- 프로필 트리 옥실 -3- 포스 포 콜린 -3- 포스 포 콜린 -3- 포스 포 콜린, 그리고이 분류의 존재 또는 결석을 가지고 있음을 보여 주었다. 항균성 결과는 계면 활성제가 좋은 항균 활성을 가지고 있음을 보여 주었다.
09 유변학 적 특성
계면 활성제의 유변학 적 특성은 식품, 제약, 석유 추출, 개인 관리 및 가정 간호 제품을 포함한 다양한 산업에서의 응용을 결정하고 예측하는 데 매우 중요한 역할을합니다. 아미노산 계면 활성제의 점탄성과 CMC 사이의 관계를 논의하기 위해 많은 연구가 수행되었습니다.
미용 산업의 10 응용
AA는 많은 개인 의료 제품의 제형에 사용됩니다.칼륨 N-Cocoyl Glycinate는 피부에 온화한 것으로 밝혀졌으며 슬러지와 메이크업을 제거하기 위해 얼굴 클렌징에 사용됩니다. N- 아실 -L- 글루탐산에는 2 개의 카르 복실기가있어 수용성이 더 높아집니다. 이 AA 중에서, C 12 지방산을 기반으로 한 AA는 얼굴 클렌징에 널리 사용되어 슬러지와 메이크업을 제거합니다. C 18 체인을 갖는 AA는 스킨 케어 제품의 유화제로 사용되며, N-Lauryl Alanine 염은 피부에 자극적이지 않아 베이비 케어 제품의 제형에 사용될 수있는 크림 같은 폼을 생성하는 것으로 알려져 있습니다. 치약에 사용되는 N-Lauryl 기반 AA는 비누와 유사한 세제 및 강한 효소 억제 효능을 가지고 있습니다.
지난 수십 년 동안 화장품, 개인 의료 제품 및 제약에 대한 계면 활성제의 선택은 독성, 온화함, 터치 및 안전에 대한 온화함에 중점을 두었습니다. 이 제품의 소비자는 잠재적 인 자극, 독성 및 환경 적 요인을 잘 알고 있습니다.
오늘날 AAS는 화장품 및 개인 관리 제품의 전통적인 상대에 대한 많은 장점으로 인해 많은 샴푸, 모발 염료 및 목욕 비누를 공식화하는 데 사용됩니다.단백질 기반 계면 활성제는 개인 의료 제품에 필요한 바람직한 특성을 가지고 있습니다. 일부 AA에는 필름 형성 기능이 있고 다른 AA에는 발포 기능이 우수합니다.
아미노산은 지층 상류에서 자연적으로 발생하는 보습 인자가 중요합니다. 표피 세포가 죽을 때, 이들은 성층의 일부가되고 세포 내 단백질은 점차 아미노산으로 분해된다. 그런 다음이 아미노산은 지층 코네움으로 더 옮겨져 지방 또는 지방 같은 물질을 표피 지층 코네움에 흡수하여 피부 표면의 탄성을 향상시킵니다. 피부의 천연 보습 인자의 약 50%는 아미노산과 피 롤리돈으로 구성됩니다.
일반적인 미용 성분 인 콜라겐에는 피부를 부드럽게 유지하는 아미노산도 포함되어 있습니다.거칠기 및 둔함과 같은 피부 문제는 대부분 아미노산 부족 때문입니다. 한 연구에 따르면 아미노산을 연고를 완화시키는 피부 화상을 완화하고 영향을받는 부위는 켈로이드 흉터가되지 않고 정상 상태로 돌아 왔습니다.
아미노산은 또한 손상된 큐티클을 돌보는 데 매우 유용한 것으로 밝혀졌습니다.건조하고 모양이없는 모발은 심하게 손상된 지층 고막에서 아미노산의 농도가 감소 함을 나타낼 수 있습니다. 아미노산은 표피를 모발 샤프트로 침투시키고 피부에서 수분을 흡수하는 능력이 있습니다.아미노산 기반 계면 활성제의 이러한 능력은 샴푸, 모발 염료, 모발 연화제, 헤어 컨디셔너 및 아미노산의 존재에 매우 유용합니다. 모발을 강하게 만듭니다.
11 일 일상 화장품 응용 프로그램
현재 전 세계적으로 아미노산 기반 세제 제형에 대한 수요가 증가하고 있습니다.AAS는 더 나은 세척 능력, 폼 능력 및 직물 연화 특성을 갖는 것으로 알려져있어 세제 세제, 샴푸, 바디 워시 및 기타 응용 분야에 적합합니다.아스파르트 산-유래 양서류 AAS는 킬레이트 특성을 가진 매우 효과적인 세제로보고된다. N- 알킬 -β- 아미노에 톡시 산으로 구성된 세제 성분의 사용은 피부 자극을 감소시키는 것으로 밝혀졌다. N-Cocoyl-β- 아미노 프로피온 네이트로 구성된 액체 세제 제제는 금속 표면의 오일 얼룩에 대한 효과적인 세제로보고되었다. 아미노 카르 복실 산 계면 활성제 인 C 14 Chohch 2 NHCH 2 COONA는 또한 더 나은 세제를 갖는 것으로 나타 났으며 섬유, 카펫, 모발, 유리 등을 청소하는 데 사용됩니다. 2- 하이드 록시 -3- 아미노 프로피온 산 -N, N- 아세토 세포 산 유도체는 우수한 복잡한 능력을 갖는 것으로 알려져 있습니다.
N- (N'-long-chain acyl-β- 알라 닐) -β- 알라닌에 기초한 세제 제제의 제조는 더 나은 세척 능력 및 안정성, 쉬운 폼 파괴 및 우수한 직물 연화를위한 특허에서 Keigo와 Tatsuya에 의해보고되었다. KAO는 N- 아실 -1 -N- 하이드 록시 -β- 알라닌에 기초한 세제 제제를 개발하고 낮은 피부 자극, 높은 방수성 및 높은 얼룩 제거 능력을보고했다.
일본 회사 인 Ajinomoto는 샴푸, 세제 및 화장품의 주요 성분으로 L- 글루탐산, L- 아르기닌 및 L- 리신을 기반으로 한 독성 및 쉽게 분해 가능한 AA를 사용합니다 (그림 13). 단백질 오염을 제거하기위한 세제 제형에서 효소 첨가제의 능력도보고되었다. 글루탐산, 알라닌, 메틸 글리신, 세린 및 아스파르트 산으로부터 유래 된 N- 아실 AAS는 수용액에서 우수한 액체 세제로 사용되는 것으로보고되었다. 이들 계면 활성제는 매우 낮은 온도에서도 점도를 전혀 증가시키지 않으며, 균질 한 폼을 얻기 위해 발포 장치의 저장 용기에서 쉽게 이동할 수있다.
후 시간 : Jun-09-2022

